为什么只有吸铁的磁铁,没有磁铜或磁铝呢?
这个问题涉及对磁性的理解。
我们知道有电荷。电荷分两种,同性相斥,异性相吸。在自然界中,大部分物质(我们身边的物质)是以分子或原子的形态存在的,而分子/原子的主要性质取决于电子。
通过摩擦,物质之间可能发生电子的转移,这就是摩擦起电现象,通过摩擦起电,我们很早就知道世界上存在两种电荷。
磁性也是人们很早就认识到的一种自然现象,但和电现象不同,我们没法孤立出两种磁荷。

典型的磁现象涉及磁铁,磁铁一般是长条形的,这两端的行为很像电荷,N端和N端靠近是排斥的,而N端和S端靠近是吸引的。这让人猜测N和S就好像电荷的正或负,但我们无法把N端和S端分开,一旦强行分开,我们会得到两个磁铁,每个磁铁上都有相反的N和S。
因为这个原因,物理学家用“磁矩”,而不是磁荷来描述磁现象。但电和磁有关系,很快被法拉第等科学家发现了,简单说就是环形电流(比如电子围绕一个圆形轨道转圈)具有磁性,这让人们猜测磁性物质的分子具有环形电流,这些磁性累加起来体现为宏观的磁性。
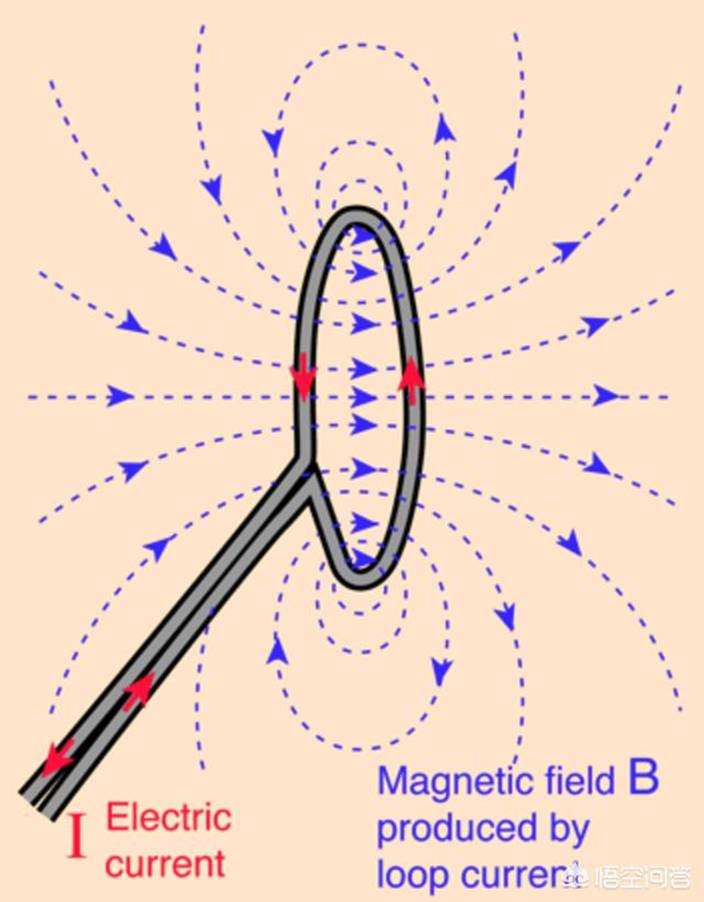
环形电流,就相当于小磁铁,也有磁矩。磁性的本质要归结到“电”,从这个角度并不存在磁铜,磁铝。因为磁铁中导致相互吸引的原因并不是只和铁有关的特别的东西,是否具有磁性需要研究物质中电子的运动状况(原子核对磁性的贡献比电子对磁性的贡献小得多)。
按照这个思路,应该在磁性物体的表面存在“环形电流”,但可惜的是这个电流并没有被人们检测到。并且人们迄今为止也没有在自然界中观察到独立的磁荷。换句话说,我们观察到的磁性现象大多都与电有关。
根据量子力学,电子在原子内的运动可以归结为四个量子数,n,l,m和sz,其中m叫磁量子数,相当于电子在原子内作“轨道运动”所具有的“轨道角动量”的z分量,如果m不是0,电子相应地会具有磁矩,这和“分子电流”的概念有点像,区别是这里电子的运动必须用量子力学来描述。
此外,根据相对论性量子力学,电子还具有内禀的自旋,它在z方向上的分量是sz,自旋也会贡献磁矩。换句话说,原子内部的电子是磁性的来源,那么为什么元素周期表上的大多数物质不体现出磁性呢?
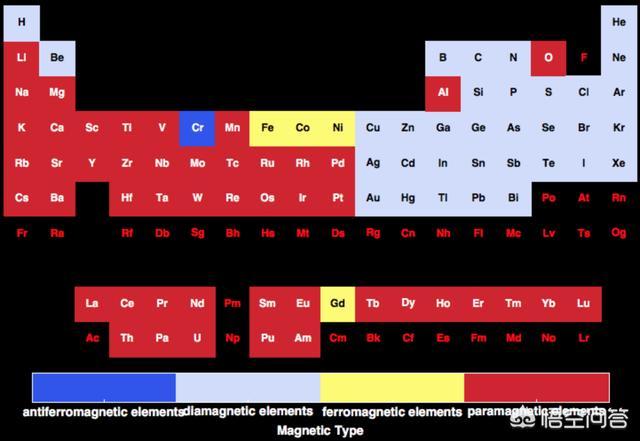
元素磁性的周期表,蓝色是反铁磁,浅蓝是抗磁,红色是顺磁,只有黄色是铁磁,对外体现出“磁性”,Gd也是铁磁的,但其居里温度只有292K(19°C),正好在室温时体现不出磁性。
一个原因是原子里面有很多电子,它们倾向于按照泡利不相容原理按照能量的高低从低到高排列,这导致大多数电子的磁矩相互抵消了,比如满壳层的电子,磁矩就互相抵消掉了。
对于固态中的原子,如果不是满壳层,则会和周围的原子形成共价键(半导体),或得失电子使得壳层变成满壳层(离子晶体),换句话说很多固态物质中的电子也不对外显示磁性了。此外,还有轨道淬灭概念,即处于晶格中的原子在特定条件下,轨道角动量的z分量平均值为0。
此外还有金属,对于金属来说,最外层电子是整个晶格共有的,它们处于一个连续的能带里,其中一半向上,一半向下,正好磁性互相抵消(铜和铝等金属就是这种情况)。除非金属的能带结构并不对称,使得某种自旋取向的电子更多,这样金属才有可能对外体现出磁性。
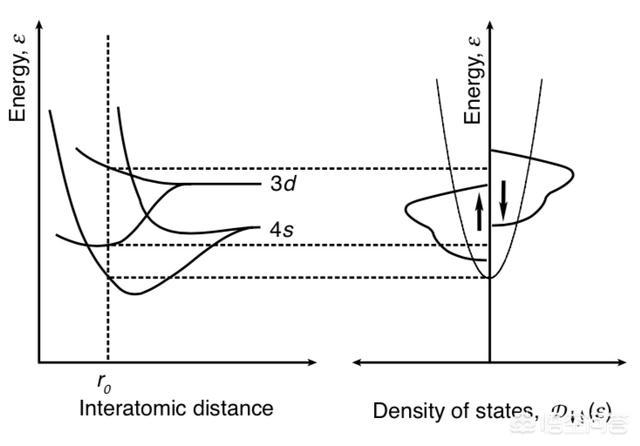
如图:4s电子对自旋向上和向下的能带是对称的,而3d电子则是不对称的。Cu的电子结构是3d^104s^1,换句话说Cu不具备磁性是因为其最外层只有4s电子。而铁(3d^64s^2)、钴(3d^74s^2)、镍(3d^94s^1)则分别都有未填充满的3d电子。铝的电子结构是3s^23p^1,因此铝也不具有磁性。
最后还要考虑居里温度(Tc),因为磁性的存在会使磁矩相互平行排列,但如果无规则热运动的能量过大,则会破坏这种平行排列,使得磁性没法对外体现出来。
换句话说,固体要对外显示出磁性,其条件是相当苛刻的,在天然物质中只有铁、钴、镍三种物质具有磁性,它们的居里温度分别是1043K,1400K和627K。
其他回答:
大学会学到,这是由元素电子结构排列式决定的。因为铁原子外层有多余的自旋单电子,而不是对电子,故原子内部磁场无法抵销,总体表现出铁磁性。同族元素金属,钴,镍同样会磁性。